Niet-metalen lijst (elementengroepen)
 Share
Share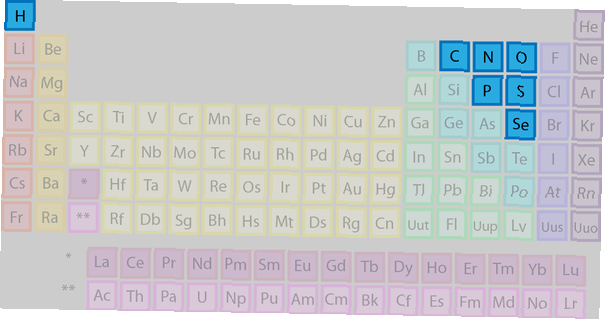
De niet-metalen zijn een groep elementen aan de rechterkant van het periodiek systeem (behalve voor waterstof, die zich links bovenaan bevindt). Ze zijn ook bekend als niet-metalen. Deze elementen onderscheiden zich doordat ze doorgaans lage smelt- en kookpunten hebben, warmte of elektriciteit niet goed geleiden en vaak hoge ionisatie-energieën en elektronegativiteitswaarden hebben. Ze hebben ook niet het glanzende "metaalachtige" uiterlijk dat bij de metalen hoort. Terwijl de metalen vervormbaar en ductiel zijn, hebben de niet-metalen de neiging broze vaste stoffen te vormen. De niet-metalen hebben de neiging om gemakkelijk elektronen te krijgen om hun schilden van valentie-elektronen te vullen, zodat hun atomen vaak negatief geladen ionen vormen. Atomen van deze elementen hebben oxidatiegetallen van +/- 4, -3 en -2.
Lijst met niet-metalen (elementengroep)
Er zijn 7 elementen die tot de niet-metalen groep behoren:
- Waterstof (soms beschouwd als een alkalimetaal)
- Koolstof
- Stikstof
- Zuurstof
- Fosfor
- Zwavel
- Selenium
Hoewel dit de elementen in de groep zijn nonmetals, er zijn twee extra elementgroepen die kunnen worden opgenomen, omdat de halogenen en edelgassen ook soorten niet-metalen zijn.
Lijst van alle elementen die niet-metalen zijn
Dus als we de niet-metalen groep, halogenen en edelgassen omvatten, zijn alle elementen die niet-metalen zijn:
- Waterstof (soms)
- Koolstof
- Stikstof
- Zuurstof
- Fosfor
- Zwavel
- Selenium
- fluorine
- Chloor
- Broom
- Jodium
- Astatine
- Tennessine (soms beschouwd als een halogeen of metalloïde)
- Helium
- Neon
- argon
- krypton
- Xenon
- Radon
- Oganesson (gedraagt zich mogelijk als een "edelgas", behalve dat het onder normale omstandigheden geen gas zal zijn)
Metalen niet-metalen
Niet-metalen worden als zodanig geclassificeerd op basis van hun eigenschappen onder normale omstandigheden. Metaalachtig karakter is geen alles-of-niets-eigenschap. Koolstof heeft bijvoorbeeld allotropen die zich meer gedragen als metalen dan niet-metalen. Soms wordt dit element beschouwd als een metalloïde in plaats van een niet-metalen. Waterstof werkt als een alkalimetaal onder extreme druk. Zelfs zuurstof heeft een metaalachtige vorm als een vaste stof.
Betekenis van de niet-metalen elementengroep
Hoewel er slechts 7 elementen binnen de niet-metalen groep zijn, vormen twee van deze elementen (waterstof en helium) meer dan 99% van de massa van het universum. Niet-metalen vormen meer verbindingen dan metalen. Levende organismen bestaan voornamelijk uit niet-metalen.
